고체 전해질과 전고체 전지(All-Solid-State Battery)
개요
산업 혁명 이후 공업과 여러가지 산업들이 빠른 속도로 발전해 나가면서, 효율적인 생산, 다양한 형태의 기술, 그리고 '에너지의 안전하고 효율적인 저장과 사용'이 산업을 발전시키는 데에 있어서 매우 핵심적인 부분을 차지하게 되었다. 특히, '배터리'는 에너지를 저장할 수 있는 장치로써, 인류가 에너지를 사용하고 산업을 발전시키는 데에 있어서 너무나도 중요한 요소다. 배터리는 갈바니 전지부터 시작하여 납축 전지, 현재는 수소 연료 전지 등 다양한 형태로 발전해 오고 있으며, 산업화의 발전에 따라 지구온난화가 진행되고 무공해 에너지에 대한 관심이 높아지면서 여러 친환경적인 에너지 사용과 배터리에 대한 관심도 높아지고 있다. 이중 가장 유명한 배터리 중 하나가 리튬-이온 전지(Lithium-ion Battery)이다. 현재 널리 쓰이는 리튬-이온 전지의 안전성 문제가 제기되면서 전해질만 고체로 바꾼 전고체 전지의 개발이 최근에 각광받고 있다. 고체 전해질이 전하를 운반하는 원리와 슈퍼 이온전도 고체 전해질의 원리를 중심으로 전고체 전지에 대한 얘기를 적어 보았다.
기존 리튬 이온 전지의 문제점
리튬-이온 배터리는 2차 전지로, 이온이 양극(환원극)과 음극(산화극) 사이를 지속적으로 이동하면서 충전과 방전이 가능하다. 그런데 기존의 리튬-이온 배터리는 액체 전해질을 사용하기 때문에 전해액이 마르거나 새어나와 화재가 발생할 수 있다. 또한 \(\ce{Li^{+}}\) 이온이 음극 표면에 존재하는 전자와 결합하여 리튬 금속 층을 형성하고 이것이 불규칙적으로 쌓여서 분리막과 양극까지 침범하여 이 역시 화재를 발생시킬 수 있다. 고체 전해질을 사용하면 전해액의 누수 가능성이 없으며, 리튬금속 층의 확장을 저지할 수 있어 이를 해결할 수 있다. 그러나 고체 전해질은 이온 전도도가 낮기 때문에 액체전해질 만큼의 효율을 낼 수 있는 고체 전해질 물질을 개발하는 기술이 주목받고 있다.
전기 전도성과 고체 전해질의 이온전도 원리
물질의 고유한 성질인 전기 전도도 \(\sigma\) 는 비저항 \(\rho\)의 역수로, 단위는 S/m이다(S는 지멘스, 옴의 역수). 고체 내에서는 결정에 존재하는 결함들을 통해서 이온이 이동하기 때문에 이온의 이동이 격자에 제한되어 있어 이온 전도도가 현저히 낮다. 액체에서는 이 결함의 크기가 매우 크기 때문에 이온이 이동하기 쉽다고 이해할 수 있다. 이온이 이 결함을 통해서 이동하기 때문에 결함이 많고 빠르게 확산하는 결정이 높은 이온 전도도를 가진다. 결함의 확산 계수는 \(D=D_{0}e^{\frac{-E_{a}}{RT}}\)로 나타나기 때문에 전기전도도 \(\sigma\)는 (-활성화에너지)의 지수함수로 나타난다다. 이때 \(R\)은 기체 상수, \(T\)는 캘빈 온도, \(E_{a}\)는 빈자리 형성 활성화 에너지이다. 따라서 이온전도도가 높은 물질을 만들려면 이온이 이동하면서 결함을 생성하는데 필요한 활성화 에너지를 낮춰야 한다. 결함의 확산은 반응 속도론에서 다루는 열 활성 과정이기 때문에 이는 아레니우스 식의 속도 상수와 유사한 형태이다.
고체 결정의 구조에는 다양한 구조가 존재하는데, 원자들의 배열을 묶는 단위인 단위세포의 모양에 따라 입방정계(정육면체), 육방정계(육각기둥) 등이 있다. 또한 단위세포에 추가적인 격자점이 있는 것을 중심의 위치에 따라 원시(없음), 체심(부피 중심), 면심(면 중심), 측심(측면)으로 분류한다. 전고체 전지에 쓰이는 고체 전해질은 주로 리튬-황화물로, 이들은 대부분이 체심입방구조(body-centered cubic, bcc)와 면심입방구조(face-centered cubic, fcc)혹은 육방밀집구조(hexagonal closed-packed, hcp)구조이다. 이때 \(\ce{Li^{+}}\)의 이동을 황 원자들이 이루는 기하적 구조의 중심에서 또 다른 중심으로 계속 이동하는 것으로 이해할 수 있다.
bcc 구조는 체심 원자 2개와 꼭짓점 원자 2개가 정사면체 구조(Tetrahedral, T)를 이룬다. 따라서 \(\ce{Li^{+}}\) 의 이동 경로는 T-T 경로만 가능하다. T-T는 정사면체에서 정사면체로 이동한다는 뜻이다. fcc는 면심 원자 6개가 정팔면체(Octahedral, O)를 이루고 그 양옆에 정사면체가 있어 T-O-T 경로가 가능하다. hcp구조는 T-O-T, T-T, O-O가 모두 가능하다. 이때 T보다 O를 지나가는 경로의 활성화에너지가 더 높은데, 그 이유는 정팔면체 구조가 더 여러 방향에서 황 원자가 리튬 이온을 끌어당기고, 정사면체 구조보다 부피도 크기 때문에 결합이 매우 안정하여 이를 끊어내기 어렵기 때문이다. 따라서 활성화에너지가 낮은 순으로 나열하면 T-T, T-O-T, O-O 순이고, T-T만을 가지는 bcc구조가 \(\ce{Li^{+}}\)의 이동도가 가장 높다.
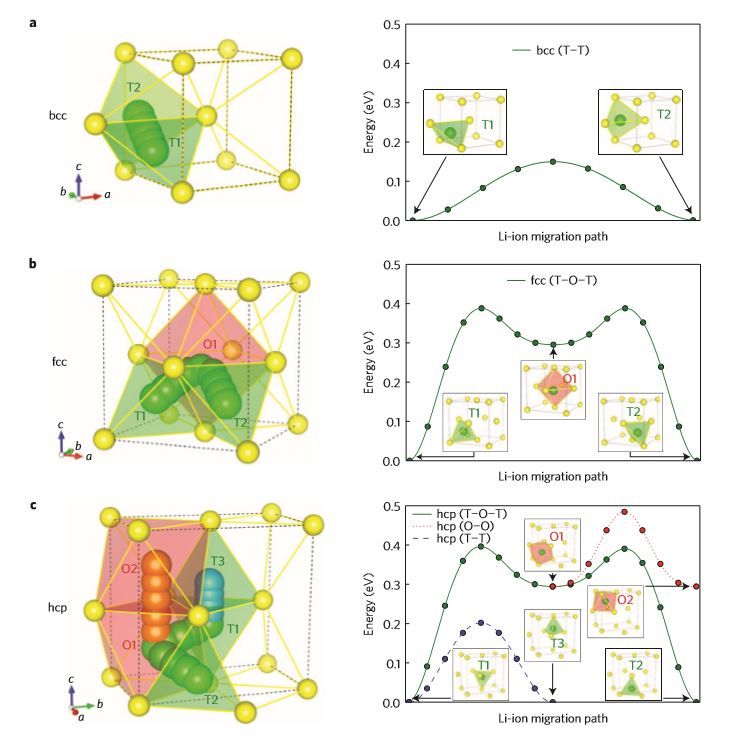
그림2에서 초록색 입체도형은 정사면체를, 빨간색 입체도형은 정팔면체를, 그 사이의 동그라미들은 이동하는 \(\ce{Li^{+}}\), 노란색 동그라미는 결정의 격자점이다. 그래프를 보면 bcc의 T-T가 가장 낮은 활성화 에너지를 가지므로 bcc형태의 결정을 갖는 리튬-황화물이 전도도가 큰 것을 알 수 있다.
한국과학기술원 KIST, 슈퍼전도성 고체 전해질 개발
한국과학기술원 KIST에서 최근 개발하여 주목 받고 있는 슈퍼 이온전도성 고체전해질은 \(\ce{Li_{7-x}PS_{6-x}Cl_{x}}\)이다. 이 물질은 \(\ce{LiPS6}\), ‘리튬-아지로다이트’라는 물질의 일부를 염소로 대체하여 만든 물질이다. 리튬-아지로다이트는 원래 fcc 구조여서 리튬 이온이 이동 중에 황 원자 팔면체 안에 갇히게 된다. 그런데 이 물질의 일부를 염소로 대체하면 정전기적 인력의 세기가 다르기 때문에 균열이 생기고 bcc형태와 또 다른 결정 구조가 생겨서 활성화 에너지가 매우 낮아짐과 함께 리튬이온의 이동에 있어서 새로운 경로가 확보된다. 연구에 따르면 염화이온의 농도가 \(x=1.5\)정도일 때의 이 물질의 이온전도도가 10.2(mS/cm)로 기존 액체전해질의 이온 전도도와 비슷하다고 한다.
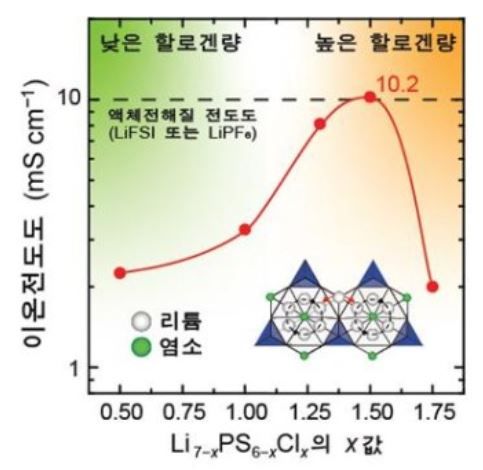
전고체 전지의 산업적 가치와 에너지밀도
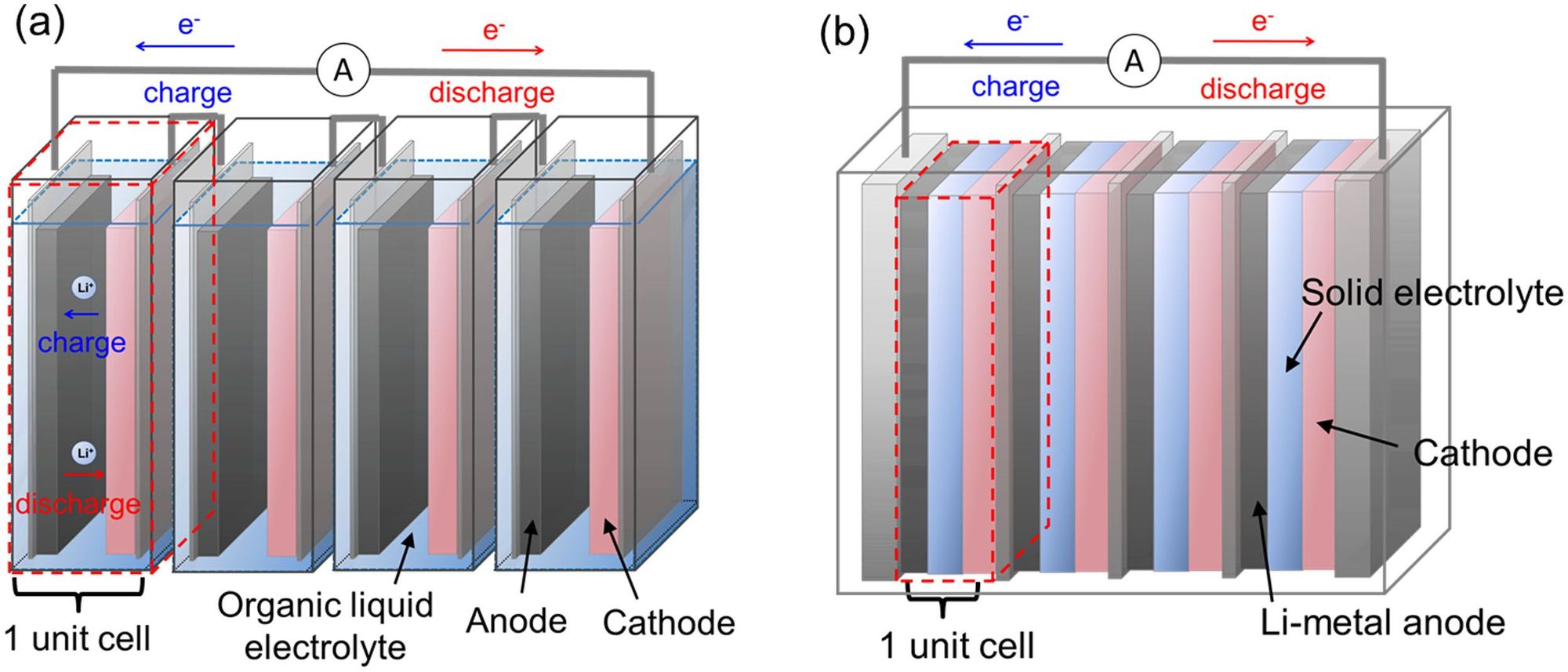
고체 전해질을 사용하면 기존의 리튬-이온 전지가 지녔던 화재와 폭발 위험을 차단하여 안전성이 매우 높다. 또한 고체 전해질로 배터리를 만들면 그림3과 같이 전극을 한꺼번에 묶어서 제조할 수 있어 액체 전해질 배터리에 비해 최소 70% 이상 증가한 에너지밀도를 가지며 배터리 소형화 측면에서 크게 앞선다. 현재 다양한 고체 전해질 물질의 개발이 빠르게 진행되고 있으며, 자동차·핸드폰 등의 전자기기에 매우 유용하게 쓰일 것으로 예상된다.
참고 문헌
I)David.W.Oxtoby, The principle of Modern Chemistry 7th edition, 2014. II)KIST 김형철 책임연구원, Superionic Halogen-Rich Li-Argyrodites, 2020. III)조윤상, 전고체 리튬 2차 전지 현황 및 국내·외 개발 동향, 2018. IV)Yan Wang외 7명, Design principles for solid-state lithium superionic conductors, 2015.
