치사율 100%인 인수 공통 전염병이 있다? [광견병]
우리는 현재 COVID-19의 창궐로 고통을 받고 있다. 하지만 코로나 바이러스의 치사율은 그렇게 높지 않다. WHO가 발표한 자료에 의하면 작년 기준으로 3.3%정도를 상회할 수준이다. 사실 이정도의 치사율을 가지는 것에는 나름의 이유가 있다. 바이러스의 입장에서는 자신들의 유전자를 널리 퍼뜨리는 것이 목적이기 때문에 적절한 치사율을 통해 숙주의 생명의 유지시키면서 복제를 해야 한다(리처드 도킨스의 '이기적 유전자'를 읽어보면 좀더 와닿을 수 있다). 하지만 이에 반해 광견병은 거의 100%의 치사율을 가지는 엄청난 전염병이다[1]. 광견병이 이러한 치사율을 가질 수 있는 이유에는 긴 잠복기, 그리고 야생으로부터 유래된 질병이라는 점이 유리하게 작용한다. 치사율이 높더라도 숙주가 오랜 잠복기동안 질병을 퍼뜨릴 수 있고 야생에서의 감염이 빈번하게 일어나기 때문이다.
앞의 이야기만 들어보면 광견병이라는 것이 다른 나라의 이야기라고 생각할 수 있다. 물론 국내에서는 개에게 물려서 광견병이 발생했다는 케이스가 거의 나타나고 있지는 않지만 야생동물에게는 충분히 감염될 위험이 있고 우리나라에서 아직 완전히 사라진 질병이라고 하기도 힘들다. 광견병은 우리가 운이 나쁘다면 일상생활, 혹은 해외여행을 갔을 때 마주칠 수 있지만, 반대로 철저한 대비와 예방을 통해 충분히 막을 수 있는 질병이다. 이 무시무시한 광견병에 대해 C. E. Rupprecht, C. A. Hanlon, and T. Hemachudha, “Rabies re-examined,” The Lancet Infectious Diseases, vol. 2, no. 6, pp. 327–343, 2002 의 논문을 읽으면서 집중 탐구를 해보도록 하자.
광견병은 개로부터만 걸리는 병?
우선 이름부터 광견병이기 때문에 狂犬(광견)으로부터 걸리게 된다는 고정관념이 생기는 것은 당연하다. 결론부터 말하면 광견병은 광견병의 원인이 되는 리사바이러스(lyssavirus)를 가지고 있는 모든 숙주로부터 전염 가능하다. 여러 문헌들을 보면 기원전 500년에도 광견병으로 의심이 되는 증상을 보이는 동물들(특히 개들)을 목격했다는 기록이 있다. 15, 16세기 경에는 다른 대륙들로의 항해가 잦아졌고 그 과정에서 광견병은 전세계를 떠돌며 숙주들을 찾아다니게 된다.
재밌는 부분은 지금부터다. 현대 사람들이 인간의 질병을 알기 위해 비교적 만만한(?) 동물들을 희생하여 실험을 하는 것과 반대로 과거 광견병 증상을 앓는 개들이 나타나자 사람들은 병의 정체를 규명하기 위해 동물의 체액을 사형수들에게 주입하여 그 반응을 관찰했다. 당연히 체액을 주입당한 사람들은 모두 죽었다. 1804년이 되어서야 독일의 과학자 Zinke는 광견병이 동물의 침 등을 통해 체내로 유입되어 전파가 된다는 사실을 밝혀냈고 1879년 Galtien은 실험적으로 광견병을 토끼에게 유발하는데 성공했다. 이처럼 광견병은 개를 비롯한 아주 다양한 동물로부터 전파될 수 있고 특히나 밀림 지역에서 박쥐에 의해 전파되는 경우도 빈번하다.
병원균의 다양성
광견병을 옳기는 병원균은 리사바이러스(lyssavirus)이다. 리사바이러스는 속명으로(genus) 유전적으로 관련이 되어 있는 바이러스들의 모임이다. 유전자형의 종류가 적어도 7개는 있다고 한다.
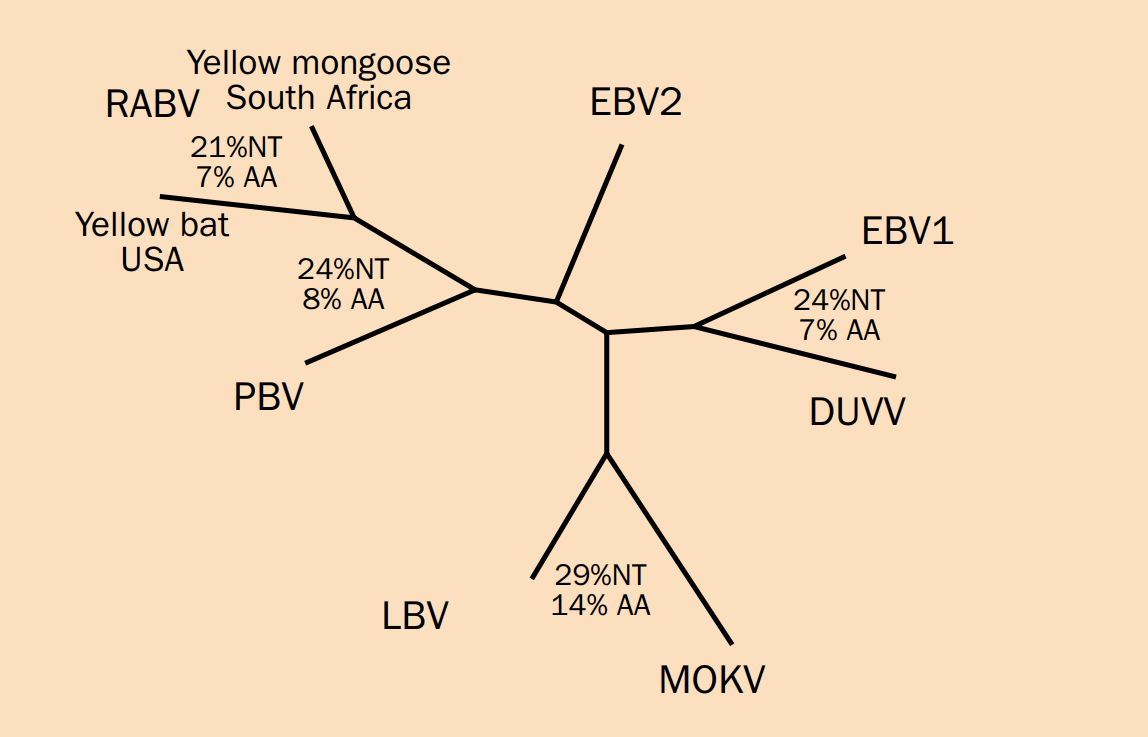
리사바이러스는 매우 치명적이라서 증상이 발현되면 거의 죽는다고 할 수 있다. 그래서 증상 발현을 예방하는 이런저런 방법들을 사용하게 된다. 이때 위와 같이 바이러스의 유전자형이 다양하다는 것은 한 가지 종류의 항체만을 사용한다고 했을 때 문제가 될 수 있다. 그렇기에 항원형(serotype)가 같은 묶음끼리 교차반응이 가능하다는 것을 이용하여 특정 항원형에 속하는 바이러스에 대응할 수 있는 항체를 사용함으로써 여러 타입들을 한꺼번에 억제할 수 있게 된다. 물론 다른 항원형에 속하는 바이러스에 감염된 것이라면 그에 따른 항체를 사용해야 한다.
병원균의 성질
리사바이러스는 포유동물의 중추신경계에서 생활을 할 수 있도록 진화했다. 75nm~200nm의 크기를 가지며 총알의 형태를 가졌다. 눈치챘을 수도 있겠지만 기사 커버로 사용된 바이러스 사진이 리사바이러스이다.
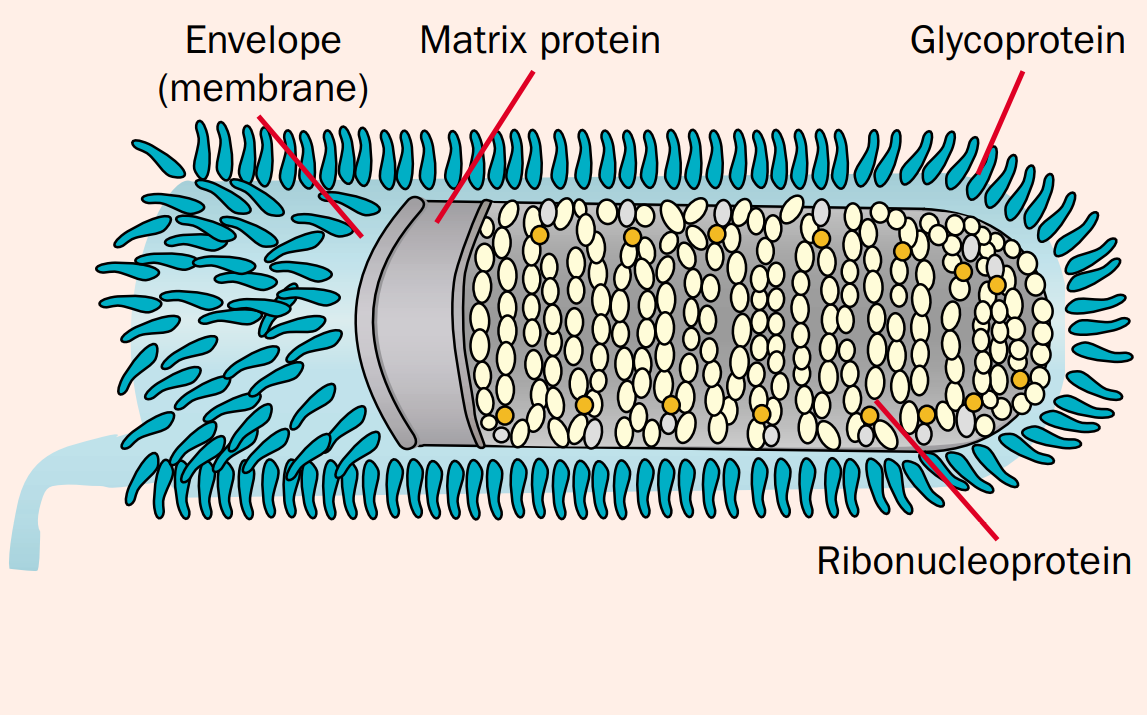
조금 더 자세히 볼 수 있게 논문에 있는 그림을 첨부했다. 얇은 막(membrane)의 바깥쪽에는 뉴클레오캡시드(nucleocapsid)가 이를 둘러싸고 있다. 핵산을 둘러싸고 있다고 해서 뉴클레오캡시드이고(바이러스의 유전체가 DNA일지 RNA일지는 모르게 때문에 nucleo) 어떻게 보면 진핵생물에서의 히스톤 단백질과 비슷한 느낌이라고 할 수 있겠다[2]. 차이점은 뉴클레오캡시드는 유전체의 겉부분을 둘러싼다는 것. 이것 외에는 기본 조직과 생식은 일반적인 바이러스와 크게 다르지 않다.
특징적인 것은 다섯개의 모노시스트론 유전자들이(monocistronic genes) 각각 5개의 단백질을 발현하는데에 관여한다는 것이다. 보충 설명을 하자면 모노시스트론은 프로모터(promoter)와 종결부위(terminator) 사이에 하나의 유전자가 존재하는 것으로 우리가 알고 있는 젖당 오페론과 같은 폴리시스트론(polycistron)과는 대비되는 용어이다. 한편 각각의 유전자는 특정 기능을 하는 단백질을 암호화한다[3].
N gene: viral DNA를 감싸는 nucleoprotein을 암호화
P gene: phosphoprotein을 암호화
M gene: matrix protein을 암호화
G gene: glycoprotein을 암호화
L gene: RNA polymerase를 암호화
N, P, M, G, L의 유전자 형태는 다른 몇몇 바이러스(특정 계통수)에서도 공통으로 나타나는 형식이라서 수포성 구내염 바이러스(vesicular stomatitis virus)에서도 발견할 수 있다. 이 특정 유전자들은 그 계통에서 공통적으로 가지고 있고 추가적인 유전자의 유무로 더 세세하게 종류가 나뉘게 된다.
이런 분자생물학적 특성 말고도 lyssavirus는 거의 모든 포유류에 서식할 수 있고 특히나 가장 주된 숙주는 개들이다. 아래의 그림은 lyssavirus가 어떠한 방식으로 세포 속으로 들어가고 나오는지를 나타낸 것이다.
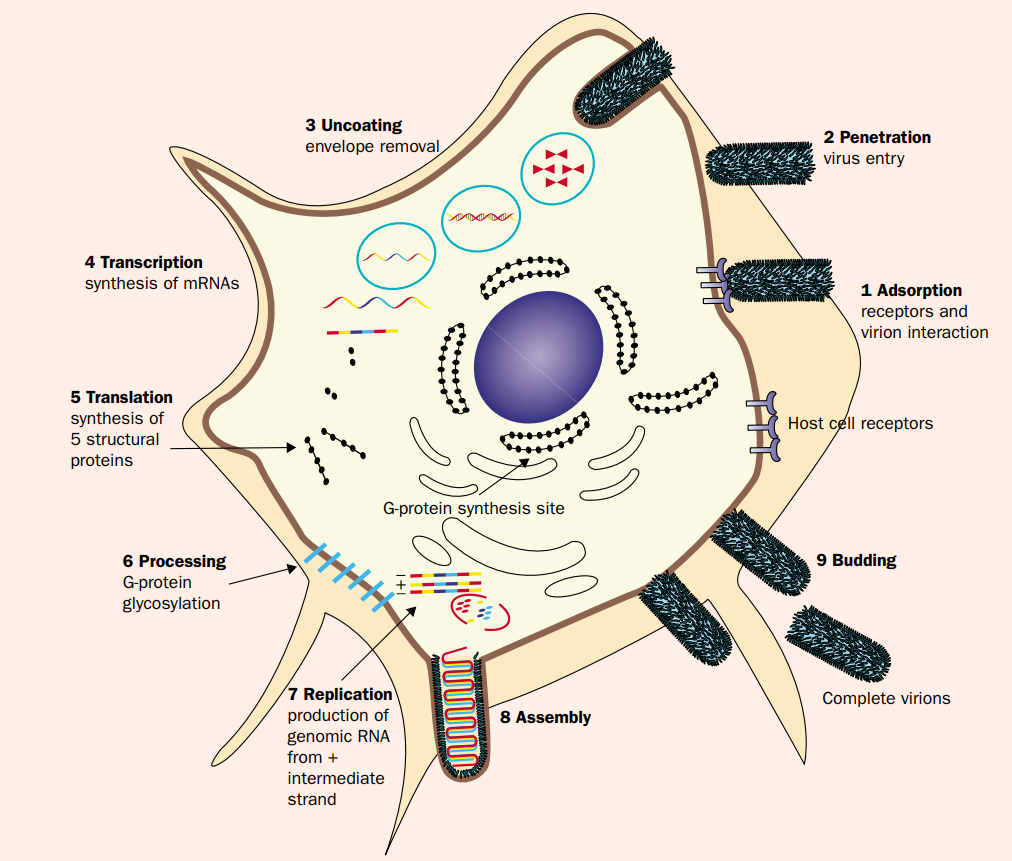
lyssavirus의 활동을 크게 9개의 단계로 나누는 것을 알 수 있다. 1단계인 absorption에서는 숙주 세포의 수용체와 virion이라는 부분이 상호작용하는 것을 알 수 있다. virion은 바이러스가 숙주 세포 외에 존재할 때의 형태를 말하는 것으로 증식은 불가능하지만 감염력은 가지고 있는 상태를 일컫는다. penetration을 통해 바이러스가 세포 속으로 들어가면 겉의 단백질 피막을 제거하면서 유전체만 남게 된다. RNA로부터 N, P, M, G, L protein이 만들어지는 과정을 자세히 살펴볼 필요가 있다. W. H. Wunner and K.-K. Conzelmann, “Rabies Virus,” Rabies, pp. 17–60, 2013. 을 보면 lyssavirus는 RNA 바이러스이지만 역전사 과정을 거치지 않고 RNA 자체에서 mRNA와 그 복제본을 전사하는 과정을 취한다.
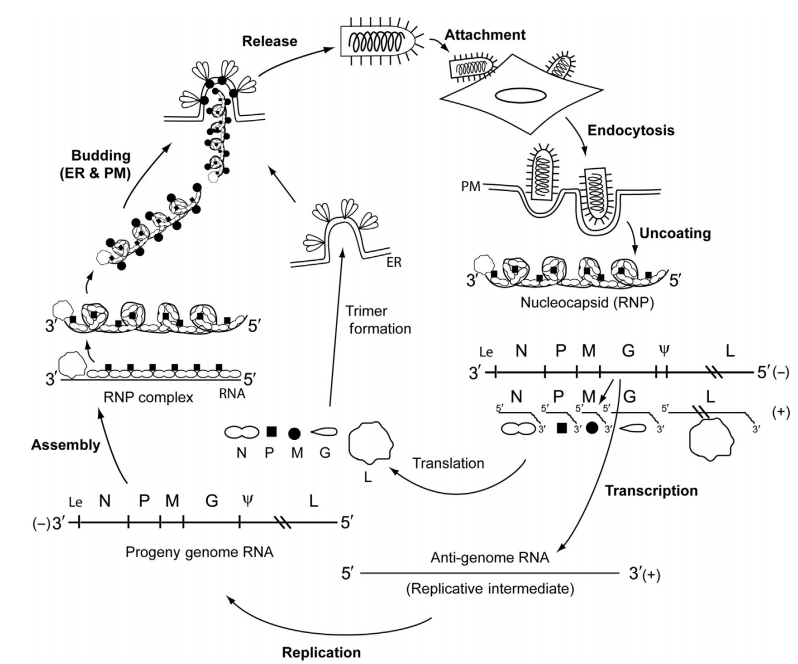
이 버전의 그림을 보면 전사 과정에 대한 이해가 쉬울 것 같다. RNA에는 +가닥과 -가닥이 존재한다. 이때 +가닥이 주형 가닥으로 +에서만 다른 유전체가 전사되거나 번역을 통해 단백질을 만들어낼 수 있다. 그렇기에 처음의 -가닥에서 단일 시스트론의 5개의 mRNA(+가닥)이 전사되고 마찬가지로 +가닥의 cRNA가 만들어진다. mRNA로부터는 N, P, M, G, L protein이 만들어지고, cRNA로부터는 복제를 통해 -가닥의 RNA가 생성된다. 이때 만들어진 -가닥과 N, P, M, G, L protein들이 합쳐지면서 온전한 lyssavirus를 이루게 되고 숙주 세포의 밖으로 나가서 다른 세포로 들어가게 된다.
그림 3을 보면 G-protein glycosylation 과정이 있는데 이는 lyssavirus가 막에 위치한 G-protein에 일종의 가공을 거쳐서 바이러스가 세포 밖으로 나갈 수 있도록 하는 과정이다. 위의 복잡한 과정들을 통해 lyssavirus는 신경세포들을 타고 CNS(중추신경)으로 이동해서 숙주를 죽음에 이르게 하는 것이다.
예방과 치료
일단 증상이 발현되면 끝난것이다. 하지만 광견병이 의심되는 개에게 물렸을 경우 그 즉시 치료만 잘 해준다면 생존할 수 있다. 안타까운 것은 많은 광견병 케이스들이 적절한 약품만 있으면 치료가 가능한 반면 세계 여러 개발도상국에서는 이러한 약품들의 부재로 인해 생존률의 차이가 어마어마하다는 것이다.
예방의 첫 시작은 놀랍게도(?) 교육을 하는 것 부터이다. 위험지역, 감염 경로에 대한 교육이 필수적이고 특히나 광견병은 물림에 의해서만 감염이 된다는 사실을 알고 있어도 도움이 된다. 그리고 나서 백신을 사용하는데 예방백신을 사람이 아닌 동물을 대상으로 많이 접종한다. 애초에 사람이 사는 지역까지 바이러스를 옮기는 것을 막으려는 의도이다.
광견병 바이러스를 보유한 동물에게 물렸다면 빠른 대응이 필요하다. 상처 부위를 비누와 아주 많은 양의 물로 씻어내는 것부터가 아주 중요하다. 체내로 유입되는 바이러스의 수를 줄일 수 있는 기회이기 때문이다. 그리고는 human rabies immunoglobulin을 지속적으로 투여를 해준다. 면역 반응에 의해 광견병 증상의 발현을 막을 수 있다.
더 나아가서
미시적인 치료법에 대한 연구도 중요하지만 동물들과 사람들의 접촉을 관리하는 것이 가장 실질적인 해결 방안이고 백신 정책을 정비하는 것도 좋은 방법이 될 것이다. 우리나라에서는 광견병 백신 접종이 의무화되어 있기 때문에 주기에 맞게 반려동물에게 백신을 주사하면 반려동물에게 물려서 감염될 걱정을 덜 수 있다. 최근에는 lyssavirus를 개조하여 신경세포의 기능을 확인하는 rabies tracing 기술도 개발 중인 것 처럼 오히려 이 바이러스가 신경세포를 감염시킨다는 것을 이용하여 신경 분야의연구의 진행도 기대할 수 있을 것 같다[4].
참고문헌
C. E. Rupprecht, C. A. Hanlon, and T. Hemachudha, “Rabies re-examined,” The Lancet Infectious Diseases, vol. 2, no. 6, pp. 327–343, 2002(내용, 그림1, 그림2, 그림3)
W. H. Wunner and K.-K. Conzelmann, “Rabies Virus,” Rabies, pp. 17–60, 2013.(내용, 그림4)
[1]http://www.amc.seoul.kr/asan/healthinfo/disease/diseaseDetail.do?contentId=31609
[2]https://terms.naver.com/entry.naver?docId=5894470&cid=61232&categoryId=61232
[3]https://terms.naver.com/entry.naver?docId=5751507&cid=61233&categoryId=61233
[4]T. J. Roelofs, S. Menting-Henry, L. M. Gol, A. M. Speel, V. H. Wielenga, K. M. Garner, M. C. Luijendijk, A. A. Hennrich, K.-K. Conzelmann, and R. A. Adan, “Optimization of whole-brain rabies virus tracing technology for small cell populations,” Scientific Reports, vol. 11, no. 1, 2021.
